Receber o diagnóstico de metástase, isto é, o espalhamento do câncer para além do local primário por vias sanguíneas ou linfáticas, é uma péssima notícia para aqueles que sofrem com a doença. Não deveria ser diferente: em cerca de 90% dos casos, há óbito do paciente. É isso que motiva a professora Claudiana Lameu, do Instituto de Química da USP (IQ-USP) a encontrar soluções – e esta pode vir de um corante alimentício, o Azul Brilhante G.
O grupo da docente desenvolve pesquisas com três tipos de câncer: o neuroblastoma, câncer extracranial sólido mais comum entre pacientes infantis; tumor de pulmão e o glioblastoma. Em trabalho publicado em maio deste ano, Kinin and Purine Signaling Contributes to Neuroblastoma Metastasis, a equipe analisou mecanismos envolvidos na metástase do neuroblastoma, que acomete 50% dos diagnosticados com a doença.
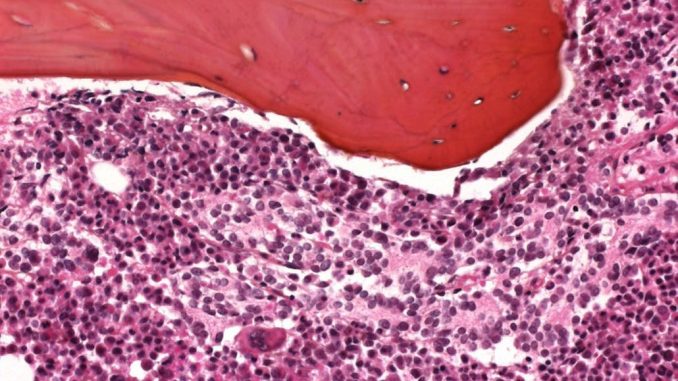
Neste estudo, que concorre a um prêmio no Instituto de Câncer de São Paulo (ICESP), verificou-se a ação metastática na medula óssea, local de preferência para formação do tumor secundário no caso do neuroblastoma. A equipe se preocupou em avaliar a interação do chamado sistema purinérgico, “um sistema de sinalização celular não muito explorado ainda, importante para situações fisiológicas, normais, desde o sistema nervoso interno, das conexões entre os neurônios até o sistema imunológico”, explica Claudiana.
O ATP (trifosfato de adenosina), molécula central do sistema purinérgico, é uma fonte de energia vital para o organismo e mantém as células vivas. No entanto, está envolvido diretamente com a ativação de receptores P2 na membrana plasmática sanguínea. A partir do trabalho, foi observado que, com o bloqueio do receptor relacionado a essa sinalização, o receptor P2X7, a atividade de metástase regride.
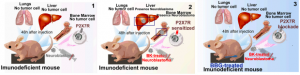
“No modelo em camundongos, quando bloqueamos esse sistema, é possível ver menos células se disseminando e, além disso, o tamanho do tumor diminui drasticamente. Observamos que, nos modelos animais, as células realmente formam metástase na medula óssea, e quando a gente bloqueia o receptor P2X7, essa metástase é drasticamente reduzida”, explica a docente.
Justamente o bloqueio do P2X7 é realizado por uma molécula chamada Azul Brilhante G (BBG, na sigla em inglês), que é utilizada pela indústria como corante alimentício. “Tanto é que nossos animais ficam com coloração azul quando são tratados com isso”, brinca a professora, indicando a necessidade de altas dosagens da droga, atualmente, para obter o efeito anti-metastático.
Em colaboração com professores da Faculdade de Ciências Farmacêuticas da USP, a equipe de Claudiana trabalha, agora, com o desenvolvimento de novas formulações para diminuir a dose efetiva para bloquear a metástase sem deixar os animais azuis. “Nossa ideia é transpor uma molécula que já está aprovada para o uso em humanos, mesmo que seja em alimentos, para a complementação de tratamentos para o câncer. Estamos trabalhando no melhoramento dessa molécula com a nanotecnologia para poder usá-la em outra aplicação, com isso pulando vários passos”, comenta Claudiana.
“Como vimos que a molécula (BBG) tem um efeito mesmo sem a melhoria na estrutura ou na formulação, apostamos que isso possa ser uma ferramenta importante de auxílio nos tratamentos de câncer, para impedir a metástase”, afirma a docente, que aposta no sucesso do corante nanoparticulado.
A (não) eficiência das terapias convencionais
Durante as pesquisas, Claudiana e equipe observaram a sobrevivência peculiar, por mais agressiva que seja a terapia, de células cancerígenas especiais. Segundo a professora, “essas células que são as responsáveis pela recorrência do tumor, mesmo depois que o paciente é considerado curado. Acredita-se que tem uma população de células resistentes que podem ficar em estado dormente no organismo”. O grupo estuda os sinais e processos biológicos envolvidos nesse “estado dormente” e na proliferação dessas células.
Além disso, os pesquisadores observaram que, na medula óssea, as terapias convencionais, isto é, a quimioterapia e a radioterapia, induzem a liberação de substâncias que são “atratoras” para as células cancerígenas. Ou seja, “o próprio tratamento não só não combate as células que são metastáticas como também proporcionam um ambiente favorável para o crescimento e atração dessas células para o nicho metastático”.



Faça um comentário